현재 국내에서 골다공증 치료에 가장 많이 사용되고 있는 약물과 차별화된 임상적 유용성과 복약편의성을 제공하는 바이오약물이 급여권에 진입해 향후 골다공증 치료 패러다임 전환이 전망된다.
오는 10월 1일부터 건강보험 급여가 적용되는 암젠코리아의 ‘프롤리아(성분명: 데노수맙)’가 그 주인공으로, 최초이자 유일한 ‘RANKL 표적’ 골다공증 치료제다.
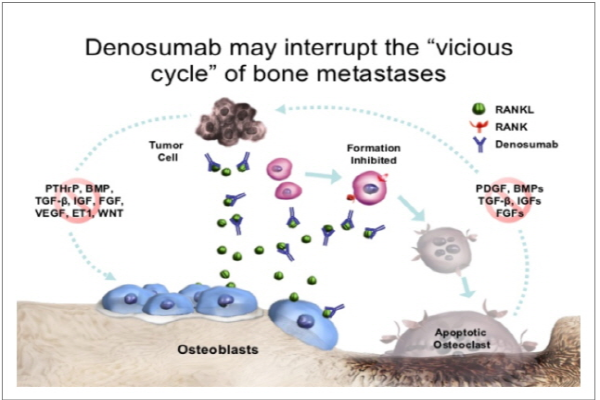
뼈를 파괴하는 파골세포의 형성과 활성화 및 생존에 필수적인 단백질인 RANKL(Receptor Activator of Nuclear factor Kappa-B Ligand)은 파골전구세포에서 발현되는 RANK와 결합해 파골세포의 형성, 활성화, 생존을 증가시킨다.
단일클론항체 의약품인 프롤리아는 이러한 RANKL을 표적해 파골세포의 형성, 활성화, 생존을 억제하고, 파골세포가 뼈에 도달하기 전에 활동을 억제함으로써 결과적으로 골 흡수를 효과적으로 억제하는 기전을 지녔다.
또한, 혈액과 세포외액을 순환하며 해면골 뿐만 아니라 피질골 모두에서 강력하면서도 가역적인 골흡수 억제 및 골밀도 증가 효과를 나타낸다.
프롤리아는 지난 2010년 미국 FDA와 EU 집행위원회의 승인을 받았으며, 국내에서는 2014년 9월 식약처 시판허가를 획득한 후 지난해 11월 비급여 출시됐다.
프롤리아는 최근 발표된 10년 장기임상에서 우수한 골절 예방과 골밀도 개선 효과를 나타냈을 뿐 아니라 이미 해외에서 충분한 처방경험을 쌓으며 효과와 안전성을 입증했다.
주요 임상데이터를 보면, 프롤리아는 3년에서 10년까지의 임상연구 결과 위약과 비교해 주요 골격 부위의 골절 위험을 각각 척추 68%, 고관절 40%, 비척추 20% 감소시킨 것을 물론, 10년간 지속적으로 골절 발생률이 낮게 유지됐다.
프롤리아는 10년간 장기 치료 시에도 치료적 정체 없이 지속적이고 우수한 골밀도 개선 효과를 보인 데이터도 보유하고 있다.
또, 10년간 진행된 임상연구에서 장기 투여 시에도 악성 종양, 감염, 심각한 감염의 발생이 낮게 유지되는 것으로 나타났다. 이와 같은 프롤리아의 안전성은 암젠의 약물 부작용 감시 프로그램을 통해 지속적으로 관찰되고 있다.
특히, 프롤리아는 6개월에 1번 투여하는 피하주사제로 약물의 투여를 위해 공복, 복용 후 30분에서 1시간 동안 눕지 않기, 물과 반드시 함께 복용하기 등의 엄격한 제한사항이 없어 환자의 복약순응도가 높다.
반면, 현재 국내에서 가장 많이 사용되고 있는 골다공증 치료제인 비스포스포네이트 제제(시장점유율 80%)의 경우 ▲공복에만 투여 가능 ▲곧게 선 자세 유지 ▲장기적 투약에 대한 거부 ▲잦은 복용의 불편함 ▲부작용(감기몸살 증상ㆍ신장기능 저하ㆍ결막염 증상ㆍ턱뼈 괴사ㆍ비전형적 대퇴골 골절) 등의 이유로 인해 치료 12개월 이후 약 70%의 환자에서 치료 중단이 발생하고 있는 것으로 알려졌다.
골절이 한 번 발생하면 재골절 위험 증가와 함께, 보행능력 저하, 2차 합병증으로 인한 증상 악화, 고관절 골절 발생, 심각한 활동성 저하 등을 초래할 뿐 아니라 1년 이내 사망률이 약 20%에 달해 적극적인 치료를 통해 골다공증성 골절을 방지하는 것이 중요하다.
한편, 프롤리아 급여 적용 대상은 ▲비스포스포네이트 제제를 1년 이상 충분히 투여했음에도 새로운 골다공증성 골절이 발생하거나, 1년 이상 투여 후 골밀도 검사 상 T-score가 이전보다 감소한 경우 ▲신부전, 과민반응 등 비스포스포네이트 제제 금기에 해당하는 경우다.
또, 투여 기간은 1년에 2회이며 추적검사에서 T-score가 -2.5 이하이거나 골다공증성 골절이 발생해 약제 투여가 계속 필요한 경우 추가 2년까지 급여 혜택을 받을 수 있다.
프롤리아의 보험약가는 21만 5,678원(6개월에 1회 투여)이며, 요양기관에 따른 환자 부담금은 ▲상급종합병원 12만 9,407원 ▲종합병원 10만 7,839원 ▲병원 8만 6,271원 ▲의원 6만 4,703원 ▲원내환자 4만 3,136원 등이다.

